|
KANKER
KANKER in VOGELVLUCHT
Hieronder worden de tien meest voorkomende vormen van
kanker met hun behandelingen en hun vooruitzichten kort besproken.
Borstkanker
Per jaar wordt bij ruim 12.000 vrouwen borstkanker (mammacarcinoom)
vastgesteld. In ons land heeft een vrouw een kans van een op acht om ooit
in haar hele leven borstkanker te krijgen. Daarmee is het de meest voorkomende vorm van kanker. Jaarlijks
overlijden ongeveer 3200 vrouwen eraan. Hoewel borstkanker op alle leeftijden
kan voorkomen, is 75% van de vrouwen bij wie borstkanker wordt ontdekt, is 50
jaar of ouder.
 In 90 procent van de gevallen beginnen de kankercellen te groeien in het
melkklierweefsel van de borst. Na verloop van tijd kunnen de kwaadaardige cellen
doorgroeien in het weefsel dat de melkkliertjes omringt. Als ze losraken, kunnen
uitzaaiingen ontstaan in de lymfeklieren van de oksel. In een latere fase kunnen
ook in andere weefsels en organen uitzaaiingen voorkomen, zoals longen, botten,
hersenen, lever en huid. In 90 procent van de gevallen beginnen de kankercellen te groeien in het
melkklierweefsel van de borst. Na verloop van tijd kunnen de kwaadaardige cellen
doorgroeien in het weefsel dat de melkkliertjes omringt. Als ze losraken, kunnen
uitzaaiingen ontstaan in de lymfeklieren van de oksel. In een latere fase kunnen
ook in andere weefsels en organen uitzaaiingen voorkomen, zoals longen, botten,
hersenen, lever en huid.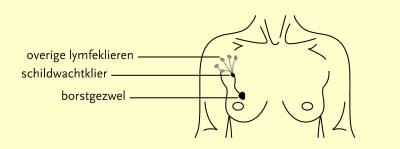
Een duidelijke oorzaak voor het ontstaan van borstkanker is niet gevonden. Wel
is duidelijk dat vrouwelijke geslachtshormonen (oestrogenen) een rol
spelen. In 5 tot 10 procent van de gevallen is er een erfelijke aanleg. Meestal
komt de ziekte dan op wat jongere leeftijd voor en vaker in beide borsten.
Omdat de tumorcellen vrij langzaam groeien, heeft de vrouw in het begin weinig
klachten. Als er een knobbeltje voelbaar wordt, gaan de meeste vrouwen naar de
huisarts, die na onderzoek een röntgenfoto (mammografie) en eventueel een
echogram zal laten maken. Een derde onderzoek is een punctie: daarbij kunnen
afwijkende cellen uit de tumor worden aangetoond. De laatste jaren wordt soms
ook gebruik gemaakt van MRI ('Magnetic Resonance Imaging': een onderzoek
dat gebruik maakt van een magneetveld in combinatie met magneetgolven en een
computer). Het is dan mogelijk om de precieze uitbreiding van de tumor in de
borst vast te stellen.
Behandeling
De primaire en beste behandeling is een borstamputatie of
een borstsparende operatie. Ongeveer 60 procent van de vrouwen kiest voor
dit laatste. Bij beide behandelingen worden ook de lymfeklieren in de oksel
operatief verwijderd als de ‘schildwachtklier’ tumorcellen bevat (zie figuur).
Afhankelijk van het stadium van de ziekte en de eventuele aanwezigheid van
uitzaaiingen wordt de patiënt aanvullend behandeld, bijvoorbeeld met bestraling,
cytostatica,
antihormonen,
proteïnekinaseremmers en/of
monoklonale antistoffen (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'). De
bestralingsbehandeling bestaat meestal uit ongeveer 25 tot 35 bestralingen, die
elke (werk)dag worden gegeven gedurende 5 tot 7 weken.
Cytostatica
Een
cytostaticumkuur bestaat doorgaans uit de intraveneuze (via een ader)
toediening van een combinatie van cytostatica, meestal eens per twee of drie
weken, en die zes tot acht keer wordt herhaald. Het gaat dan vaak om een combinatie van cyclofosfamide
(Endoxan®), methotrexaat (merkloos,
Ebetrex®, Emthexate®,
Injexate®,
Metoject®, MTX) en
fluorouracil (merkloos), de zogenoemde CMF-kuur, of
een combinatie van fluoruracil, doxorubicine en cyclofosfamide, de zogenoemde
FAC-kuur.
Antihormonen
Vooral bij de wat oudere patiënten (in de overgang en daarna) vormt hormonale
therapie een alternatief voor chemotherapie met cytostatica (die veel meer
bijwerkingen hebben). Met de (anti)hormonen (in feite zijn het
anti-oestrogenen)
fulvestrant (merkloos, Faslodex®) en
tamoxifen (merkloos) wordt de werking van
oestrogenen (de belangrijkste vrouwelijke geslachtshormonen)
geblokkeerd, waardoor de tumor in omvang kan afnemen.
Tamoxifen dient elke
dag oraal (dus via de mond) te worden ingenomen doorgaans gedurende twee
tot vijf
jaar; fulvestrant wordt eenmaal per maand toegediend via een injectie in
de bilspier. Andere anti-oestrogenen die bij uitgezaaide
borstkanker worden gebruikt, zijn
medroxyprogesteron
(merkloos, Depo-Provera®, Provera®) en
megestrol (merkloos).
Een andere optie is de behandeling
met zogenaamde aromataseremmers. Dit zijn stoffen die de vorming
van oestrogenen remmen, waardoor de concentraties oestrogenen nog lager
worden dan ze na de overgang al zijn. Daardoor neemt de groei van
oestrogeengevoelige tumorcellen af. Voorbeelden van aromataseremmers zijn
anastrozol (merkloos, Arimidex®),
exemestaan (merkloos, Aromasin®) en letrozol (merkloos,
Femara®,
Letroman®). Bij
vrouwen ná de overgang heeft een aromataseremmer een lichte
voorkeur boven tamoxifen vanwege de wat grotere effectiviteit. De bijwerkingen van deze beide typen
antihormonen ontlopen elkaar weinig. Verschijnselen die voortkomen uit een
oestrogeentekort zoals opvliegers, overmatig transpireren, hebben doorgaans de
overhand. Omdat men bij borstkanker bij voorkeur een
operatie uitvoert, al dan niet in combinatie met radiotherapie, worden
tamoxifen en aromataseremmers vooral gebruikt als aanvullende
(adjuvante)
behandeling om de groei van eventuele oestrogeengevoelige uitzaaiingen te
elimineren. Daarnaast kunnen bij patiënten bij wie reeds uitzaaiingen zijn
ontstaan, langdurige onderbrekingen van de kankeractiviteit (remissies)
met deze middelen worden bereikt.
Vaak wordt exemestaan (Aromasin®) gecombineerd met de
proteïnekinaseremmers everolimus (Afinitor®, Votubia®)
of lapatinib (Tyverb®), zie ook
proteïnekinaseremmers (in
het onderdeel 'Chemotherapie' in deze sectie 'Kanker').
Met deze combinatie is er nu een effectievere behandeling beschikbaar gekomen voor
vrouwen met hormoongevoelige
borstkanker (die de menopauze achter de rug hebben) met uitzaaiingen. De
nieuwere proteïnekinaseremmers zijn abemaciclib (Verzenios®),
palbociclib (Ibrance®) en ribociclib (Kisqali®).
Een nieuwe ontwikkeling is wellicht om met
antihormonen het risico op borstkanker bij nog gezonde vrouwen met een
verhoogd borstkankerrisico te verlagen. Met gebruik van
tamoxifen gedurende 5 jaar bleek het risico te kunnen
worden gehalveerd. Aromataseremmers bleken nog effectiever
en veiliger in het voorkómen van borstkanker: gebruik van
exemestaan (Aromasin®) gedurende 3 jaar reduceerde het risico met
65%. Het ging hier overigens om onderzoek bij vrouwen die hun overgang (menopauze)
reeds achter de rug hadden.
Monoklonale antistoffen
Vrouwen met geconstateerde uitzaaiingen die hormoongevoelig zijn, komen soms in aanmerking
behandeld te worden met een monoklonale antistof (soms ook wel
checkpointremmers genoemd), zoals
atezolizumab (Tecentriq®),
trastuzumab (Herceptin®) en pertuzumab (Perjeta®) (zie ook
monoklonale antistoffen
in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'), al dan niet in combinatie met een
cytostaticum van het type taxaan (zie ook
cytostatica in het onderdeel 'Chemotherapie'
in deze sectie 'Kanker'). De toediening vindt plaats via een intraveneus
infuus, doorgaans eens per drie weken gedurende een jaar. Indien de uitzaaiingen
hormoonongevoelig zijn, komt een andere monoklonale antistof in
aanmerking, namelijk bevacizumab (Avastin®).
|
overzicht medicatie
bij borstkanker |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Cytostatica |
CMF-kuur
cyclofosfamide
methotrexaat
fluorouracil
FAC-kuur
fluorouracil
doxorubicine
cyclofosfamide
|
Endoxan®
merkloos,
Ebetrex® Emthexate®,
Injexate®
Metoject®, MTX
merkloos
merkloos
merkloos
Endoxan®
|
injectievlst.:
750-2000 mg
tablet: 50 mg
injectievlst.: 2,5-100
mg/ml
tablet: 2½ en 10 mg
injectievloeistof: 50 mg/ml
injectievloeistof: 50 mg/ml
injectievloeistof:
2 mg/ml
injectievloeistof:
750-2000 mg
tablet: 50 mg |
|
Anti-oestrogenen |
fulvestrant
medroxy-
progesteron
megestrol
tamoxifen |
merkloos,
Faslodex®
merkloos,
Depo-Provera®
Provera®
merkloos
merkloos |
injectievloeistof: 50 mg/ml
injectievloeistof: 150 mg/ml
tablet: 100, 200 en 250 mg
tablet: 160 mg
tablet: 10, 20, 30 en 40 mg |
|
Aromataseremmers |
anastrozol
exemestaan
letrozol
|
merkloos,
Arimidex®
merkloos,
Aromasin®
merkloos,
Femara®
Letroman® |
tablet: 1 mg
tablet: 25 mg
tablet: 2½ mg
|
|
Monoklonale antistoffen |
|
atezolizumab bevacizumab
pertuzumab
trastuzumab
|
Tecentriq®
Avastin®
Perjeta®
Herceptin®
|
infusievloeistof:
60 mg/ml
infusievloeistof: 25 mg/ml
infusievloeistof: 30 mg/ml
infusievloeistof: 150 mg
injectievloeistof: 120 mg/ml |
|
Proteïnekinaseremmers |
|
abemaciclib everolimus
lapatinib
palbociclib
ribociclib |
Verzenios® Afinitor®, Votubia®
Tyverb® Ibrance®
Kisqali® |
tablet: 50, 100
en 150 mg
tablet: 2½, 5 en
10 mg
suspensie (als tablet): 5 mg
tablet: 250 mg
capsule:
75, 100 en 125 mg
tablet:
200 mg |
Dankzij de vroege opsporing en de huidige effectieve behandeling is
96% van de vrouwen met borstkanker na vijf jaar nog in leven en bij tumoren < 1
cm zelfs 100%. Als borstkanker
zich heeft uitgezaaid naar andere weefsels en organen, is er geen genezing
mogelijk. Het overlevingspercentage na vijf jaar is dan aanzienlijk lager.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl (KWF Kankerbestrijding)
http://www.diliguide.nl
(Kwaliteitsinstituut voor de Gezondheidszorg CBO)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Longkanker
Jaarlijks worden bijna 9000 nieuwe gevallen van longkanker vastgesteld. Met
circa 6500 nieuwe gevallen is het bij mannen na prostaatkanker de meest voorkomende vorm van
kanker. Bij vrouwen staat longkanker op de derde plaats. Terwijl bij mannen
momenteel een duidelijk dalende tendens te zien is, komt longkanker in
toenemende mate bij vrouwen voor. Dat heeft alles te maken met het feit dat
vrouwen later (vanaf de jaren zeventig en tachtig van de vorige eeuw) dan mannen
op grote schaal zijn gaan roken.
Van alle mensen met longkanker heeft 90 procent stevig gerookt. Andere oorzaken
zijn blootstelling aan bepaalde stoffen zoals asbest, arseen-, nikkel- en
chroomverbindingen en radioactieve stoffen, maar deze oorzaken vallen in het
niet bij roken. Mensen met astma of
COPD (in de
sectie 'Luchtwegen & Ademhaling') hebben een iets grotere kans dat zij
longkanker krijgen.
De klachten beginnen vaak met moeheid en gewichtsverlies. Opvallend is dat men
anders gaat hoesten, meestal wordt het rokershoestje hardnekkiger en heviger.
Soms wordt dan ook wat bloed opgegeven met het opgehoeste slijm. Andere klachten
zijn kortademigheid, heesheid, een fluitend geluid bij de ademhaling en pijn in
de borststreek.
Het lichamelijk onderzoek door de huisarts zal gevolgd worden door een
röntgenfoto van de longen, een CT-scan van de longen en bronchoscopie, waarbij
de luchtwegen van binnenuit worden bekeken. Soms wordt dan ook een stukje
weefsel weggenomen voor nader onderzoek.
Er zijn verschillende typen longkanker. Meer dan 90 procent ontstaat in de
grotere luchtpijpen (bronchiën); dergelijke gezwellen worden dan ook
bronchuscarcinomen genoemd. De twee belangrijkste vormen zijn het
kleincellig bronchuscarcinoom en het niet-kleincellig
bronchuscarcinoom, waaronder het grootcellig carcinoom. De behandeling en
de vooruitzichten van deze vormen zijn nogal verschillend. De niet-kleincellige
vorm komt bijna drie keer zo vaak voor als de kleincellige vorm. Uitzaaiingen in
de lever, hersenen, bijnieren en botten komen regelmatig voor, vooral bij het
kleincellig bronchuscarcinoom.
Behandeling
Een operatie is alleen mogelijk bij het niet-kleincellige bronchuscarcinoom, en dan alleen als de tumor nog een beperkte
omvang heeft en er geen uitzaaiingen zijn. Dan is er een reële kans op genezing.
Als een operatie niet mogelijk is, komt bestraling in aanmerking. De behandeling
is er dan alleen nog op gericht de tumorgroei af te remmen.
Chemotherapie
Patiënten met een
kleincellig bronchuscarcinoom krijgen meestal meteen een chemokuur met
cytostatica, zie ook
cytostatica (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'). De kanker kan vaak een tijdlang effectief worden onderdrukt
met combinaties waarin cisplatine (merkloos), cyclofosfamide (Endoxan®), doxorubicine
(merkloos), vincristine (merkloos), methotrexaat (merkloos,
Ebetrex®, Emthexate®,
Injexate®,
Metoject®, MTX) en etoposide (merkloos, Eposin®, Toposin®, Vepesid®) zijn
verwerkt. Soms wordt de chemokuur ook gecombineerd met bestraling, meestal om
bepaalde klachten te bestrijden. De standaardbehandeling van niet-kleincellig bronchuscarcinoom
is cisplatine in combinatie met gemcitabine (merkloos), docetaxel (merkloos,
Taxotere®) of vinorelbine (merkloos, Navelbine®). Ook een
behandeling worden met de monoklonale antistof bevacizumab (Avastin®)
in combinatie met een platina-bevattend cytostaticum wordt
tegenwoordig overwogen, zie ook
cytostatica en
monoklonale antistoffen (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker').
In 2015 werd de monoklonale antistof nivolumab (Opdivo®)
in Nederland geïntroduceerd bij de behandeling van uitgezaaid niet-kleincellig
longcarcinoom. Met deze optie leven patiënten significant vele maanden langer,
genezing is echter niet mogelijk. Daar hangt wel een stevig prijskaartje aan: €
150.000,- per jaar per patiënt! Reden voor de minister van Volksgezondheid eens
een stevig gesprek te hebben met de producent over of met een dergelijke prijs
het middel nog wel in aanmerking kan komen om vergoed te worden.
Een nieuwe ontwikkeling vormt de toepassing van zgn. proteïnekinaseremmers
bij de chemotherapie van longkanker. Proteïnekinasen zijn enzymen die
betrokken zijn bij tal van processen als deling en groei. Remming van deze
enzymen bij ongecontroleerde groei zoals bij kanker kan leiden tot vermindering
van de tumorgroei, zie ook
proteïnekinaseremmers in het onderdeel 'Chemotherapie' in deze
sectie 'Kanker'. De in 2014 verschenen afatinib (Giotrif®),
crizotinib (Xalkori®),
erlotinib (Tarceva®) en
gefitinib (Iressa®)
zijn
geregistreerd als monotherapie bij lokaal gevorderd of uitgezaaid
niet-kleincellig longcarcinoom. Wanneer resistentie tegen deze middelen
optreedt, is er sinds 2016 osimertinib (Tagrisso®), eveneens een
proteïnekinaseremmer.
|
overzicht medicatie
bij longkanker |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Cytostatica |
cisplatine
cyclofosfamide
docetaxel
doxorubicine
etoposide
gemcitabine
methotrexaat
vincristine
vinorelbine
|
merkloos
Endoxan®
merkloos,
Taxotere®
merkloos
merkloos,
Eposin®
Toposin®, Vepesid®
merkloos
merkloos,
Ebetrex® Emthexate®,
Injexate®
Metoject®, MTX
merkloos
merkloos, Navelbine®
|
infusievloeistof:
1 mg/ml
injectievloeistof:
750 en 2000 mg
tablet: 50 mg
infusievloeistof: 10-40
mg/ml
injectievloeistof:
2 mg/ml
capsule: 50 en
100 mg
infusievloeistof: 20 mg/ml
infusievloeistof: 200-2000 mg
injectievloeistof: 2,5-100
mg/ml
tablet: 2½ en 10 mg
injectievloeistof:
1 mg/ml
capsule: 20 en 30 mg
infusievloeistof: 10 mg/m |
|
Monoklonale antistoffen |
bevacizumab
nivolumab |
Avastin®
Opdivo® |
infusievloeistof: 25 mg/ml
infusievloeistof: 10 mg/ml |
|
Proteïnekinaseremmers |
afatinib
crizotinib
erlotinib
gefitinib
osimertinib |
Giotrif®
Xalkori®
Tarceva®
Iressa®
Tagrisso |
tablet: 20, 30, 40 en 50 mg
capsule: 200 en 250 mg
tablet: 25, 100 en 150 mg
tablet:
250 mg
tablet:
40 en 80 mg |
De vooruitzichten van longkanker zijn tamelijk slecht. Het percentage patiënten
dat na vijf jaar nog in leven is, is laag (18 procent). Als iemand na vijf
jaar nog leeft, is de kans op langdurige overleving groot. Alleen als een niet-kleincellig bronchuscarcinoom in een vroeg stadium wordt gediagnosticeerd,
is er een kans op genezing.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl (KWF Kankerbestrijding)
http://www.diliguide.nl
(Kwaliteitsinstituut voor de Gezondheidszorg CBO)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Dikkedarmkanker
Jaarlijks krijgen ongeveer 5700 mannen en 5100 vrouwen te horen dat ze dikkedarmkanker hebben. Vanaf 1990 is het aantal nieuwe gevallen ongeveer gelijk
gebleven, evenals het aantal sterfgevallen als gevolg van deze ziekte. Meestal
ontstaat dikkedarmkanker na het veertigste levensjaar.
In veel gevallen ontstaat dikkedarmkanker uit darmpoliepen. Dit zijn
goedaardige, al dan niet gesteelde gezwellen in de darmwand. Doorgaans ontstaan
ze in het onderste deel van de dikke darm (endeldarm). Waarom poliepen
bij sommige mensen ontaarden in kanker is niet bekend. Mensen met een chronische
ontsteking van de darmen, zoals de ziekte van Crohn en colitis
ulcerosa (zie ook
chronische
darmontstekingen in het onderdeel 'Darmaandoeningen' in de sectie 'Spijsvertering & Lever') hebben een grotere kans dat zij dikkedarmkanker
krijgen. Erfelijkheid speelt bij naar schatting 5 procent van de gevallen van
dikkedarmkanker een rol. Overgewicht, alcoholgebruik en weinig bewegen zijn
factoren die het risico op dikkedarmkanker verhogen.
De eerste klachten hebben dikwijls te maken met de stoelgang: afwisselend
verstopping en diarree, al dan niet met bloedverlies. Bloedarmoede met klachten
over moeheid en duizeligheid is ook vaak de eerste klacht. Toch wordt
dikkedarmkanker regelmatig (te) laat ontdekt, omdat de kanker al enige tijd
aanwezig is zonder klachten te veroorzaken. Als het kankergezwel dan op zeker
moment wordt ontdekt, kunnen er al uitzaaiingen naar de lymfeklieren en naar de
lever zijn ontstaan.
Om een definitieve diagnose te kunnen stellen zullen altijd een lichamelijk
onderzoek, onderzoek van ontlasting en bloed, röntgenonderzoek (met een
contrastvloeistof in het darmkanaal), inwendig kijkonderzoek (endoscopie)
en weefselonderzoek (biopsie) worden uitgevoerd.
Behandeling
De meeste patiënten met dikkedarmkanker zullen worden geopereerd om het
aangetaste deel van de darm en de bijbehorende lymfeklieren te verwijderen.
Afhankelijk van de plaats in het darmtraject waar wordt geopereerd, wordt er een
tijdelijke of een permanente kunstmatige uitgang (stoma) gemaakt. Bij een
kwart van de patiënten is zo’n stoma permanent. Bestraling wordt alleen
uitgevoerd bij kanker in de endeldarm (laatste gedeelte van de dikke darm) tot
30 cm vanaf de anus (rectum). Afhankelijk van de grootte van de tumor
wordt de patiënt kortdurend (één week) of langdurend (vijf tot zes weken)
bestraald.
Chemotherapie
Chemotherapie komt eigenlijk alleen in aanmerking bij aangetoonde uitzaaiingen
in de lymfeklieren en in de lever. Vaak wordt dan het cytostaticum fluorouracil
(merkloos) gegeven, in combinatie met folinezuur (merkloos,
Leucovorine®, Rescuvolin®,
Vorina®); dit is geen cytostaticum maar een stof die nauw
verwant is aan vitamine B11
(= foliumzuur) en de cytostatische werking van fluorouracil
blijkt te versterken. Ook wordt nogal eens het platinabevattende
cytostaticum oxaliplatine (merkloos,
Oxalisin®) toegepast al dan
niet in
combinatie met capecitabine (merkloos,
Xeloda®), zie ook
cytostatica (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'). Nieuwere middelen als de monoklonale antistoffen
zoals
aflibercept (Zaltrap®), bevacizumab (Avastin®) en cetuximab (Erbitux®) komen dan
eveneens in aanmerking, zie ook
monoklonale antistoffen (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker').
Sinds 2014 is de proteïnekinaseremmer regorafenib (Stivarga®)
geregistreerd voor de behandeling van uitgezaaide dikkedarmkanker, zie ook
proteïnekinaseremmers (in
het onderdeel 'Chemotherapie' in deze sectie 'Kanker').
ASPIRINE
Een dagelijks poedertje of tabletje aspirine zou weleens kunnen helpen bij het
voorkómen van darmkanker. Ooit ontwikkeld als pijnstiller wordt aspirine
- in een lage dosering - tegenwoordig vooral gebruikt om mensen te beschermen
tegen het optreden van herseninfarcten en hartproblemen. Bij toeval ontdekte men
een aantal jaren geleden dat patiënten die aspirine slikten vanwege deze hart- en
vaatziekten niet alleen een kleinere kans hadden op het krijgen van
dikkedarmkanker maar ook een kleinere kans om aan deze ziekte te overlijden.
Deze verrassende vondst was aanleiding om nader onderzoek te verrichten. Daaruit
bleek dat als men jarenlang laaggedoseerd (80 - 100 mg) aspirine had
geslikt, er 20 - 24% minder risico op darmkanker is te verwachten. Nog
indrukwekkender waren de resultaten van een grootschalig onderzoek uitgevoerd in
het Leids Universitair Medisch Centrum, waarbij ongeveer 14.000 patiënten waren
betrokken. In deze studie bleek dat patiënten die na de diagnose dikkedarmkanker
of een andere vorm van kanker in het spijsverteringskanaal, aspirine
slikten gemiddeld een betere overleving hadden. De kans dat ze vijf jaar na de
diagnose nog leefden was voor hen dubbel zo groot als voor patiënten die geen
aspirine gebruikten. De onderzoekers denken dat aspirine een gunstig
effect heeft doordat het de klontering van bloedplaatjes remt. Bloedplaatjes
zijn betrokken bij de stolling en losse tumorcellen verschansen zich vaak in een
klein stolsel om aan het afweersysteem te ontsnappen. Aspirine blokkeert
dat. De tumorcellen blijven toegankelijk voor afweercellen waardoor het
uitzaaien van kanker wordt voorkomen.
Toegepast als bloedplaatjesremmer (dus in een lage dosis) is aspirine
verkrijgbaar als het merkloze acetylsalicylzuur en onder de merknamen Acetylsalicylzuur Cardio® en Aspirine Protect®.
Het even werkzame carbasalaatcalcium
is het calciumzout van acetylsalicylzyuur en is
onder de merknamen Ascal Cardio®
en Carbasalaatcalcium Cardio® verkrijgbaar. Bij de hier gebruikte lage
doseringen van aspirine is de kans op bijwerkingen zoals maagklachten of
zelfs maagdarmbloedingen - die bij de hogere, pijnstillende doseringen kunnen
optreden - klein. Overgevoeligheidsverschijnselen bij met name astmapatiënten in
de vorm van huiduitslag, hooikoorts of benauwdheid kunnen wel degelijk optreden!
|
overzicht medicatie
bij dikkedarmkanker |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Cytostatica |
capecitabine
fluorouracil
folinezuur
oxaliplatine |
merkloos, Xeloda®
merkloos
merkloos, Leucovorine®
Rescuvolin®, Vorina®
merkloos, Oxalisin® |
tablet: 150,
300 en 500 mg
injectievloeistof: 50 mg/ml
injectievloeistof: 15-500 mg
tablet: 15 mg
infusievloeistof: 5 mg/ml |
|
Monoklonale antistoffen |
aflibercept
bevacizumab
cetuximab |
Zaltrap®
Avastin®
Erbitux® |
infusievloeistof: 25 mg/ml
infusievloeistof: 25 mg/ml
infusievloeistof: 5 mg/ml |
|
Proteïnekinaseremmers |
|
regorafenib |
Stivarga® |
tablet:
40 mg |
|
ASPIRINE |
acetylsalicylzuur
carbasalaatcalcium
|
merkloos
Acetylsalicylz. Cardio®
Aspirine Protect®
merkloos, Ascal Cardio®
Carbasalaatcal. Cardio® |
tablet:
80 en 100
mg
bruistablet, poeder: 100
mg
|
De vooruitzichten voor patiënten met dikkedarmkanker lopen sterk uiteen. Als het
gezwel zich beperkt tot het darmslijmvlies, kan een patiënt zich na operatie als
genezen beschouwen. De vijfjaarsoverleving is dan 80 tot 90 procent. Is het gezwel dieper ingegroeid en zijn er mogelijke
uitzaaiingen, dan is het vooruitzicht veel minder gunstig. Dan is na vijf jaar nog 60 procent in leven.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl (KWF Kankerbestrijding)
http://www.diliguide.nl
(Kwaliteitsinstituut voor de Gezondheidszorg CBO)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Prostaatkanker
Het aantal nieuwe gevallen van prostaatkanker per jaar overstijgt het aantal
mannelijke patiënten met longkanker: bij circa 9500 mannen per jaar wordt deze
vorm van kanker vastgesteld. Daarmee is
prostaatkanker de meest voorkomende vorm van kanker bij mannen. Ongeveer 2400 mannen
per jaar overlijden aan deze ziekte.
Prostaatkanker komt vrij weinig voor bij mannen jonger dan 60 jaar. Ongeveer 75% van de patiënten is ouder dan
65 jaar, en daarmee is prostaatkanker een
echte ouderdomsziekte. Van alle tachtigers heeft waarschijnlijk meer dan de helft
prostaatkanker - de meesten zonder het te weten en zonder er hinder van te
hebben. De gevleugelde uitspraak is: 'er sterven meer mannen mét prostaatkanker
dan áán prostaatkanker'.
Over de oorzaken van prostaatkanker is erg weinig bekend. Hoewel het mannelijke
hormoon (testosteron) een duidelijke invloed heeft op de groei van de
kankercellen, is de betekenis daarvan bij het ontstaan onduidelijk. Bij 5-10 procent van de patiënten is er sprake van een erfelijke factor. Is dat het
geval, dan gaat het om de meest kwaadaardige vorm van prostaatkanker die vooral
bij ‘jongere’ mannen (vóór het vijfenvijftigste levensjaar) voorkomt.
De eerste klachten bij prostaatkanker lijken veel op die bij een
goedaardige
prostaatvergroting (BPH): bemoeilijkte urinelozing en een slappe urinestraal ondanks
persen (zie ook het onderdeel 'Plasproblemen' in de sectie 'Nieren & Urinewegen').
Bloed in de urine en pijn of een branderig gevoel bij het plassen zijn zeker
redenen voor een nader onderzoek. Het is echter ook mogelijk dat de patiënt pas
klachten krijgt als er al uitzaaiingen zijn. Meestal heeft de patiënt dan
klachten over pijn in de botten, bijvoorbeeld rugpijn door uitzaaiingen in de
botten.
Prostaatkanker wordt wel eens bij toeval ontdekt als de arts bij inwendig
onderzoek via de anus een knobbelige prostaat voelt. Een patiënt met de genoemde
klachten moet in ieder geval inwendig worden onderzocht door de huisarts, waarna
de uroloog nader onderzoek zal uitvoeren. Echografie, bloedonderzoek en
weefselonderzoek (biopsie) zijn de belangrijkste technieken om vast te
stellen of er sprake is van kanker. Bij bloedonderzoek wordt het PSA-gehalte
bepaald. PSA staat voor prostaatspecifiek antigeen, een eiwit dat
alleen in de prostaat wordt gemaakt en dat bij
prostaatkanker in een sterk verhoogde concentratie in het bloed wordt gevonden.
Normaal gesproken komt deze stof in kleine hoeveelheden (een waarde van 0 tot 3
µg/l) voor in het bloed. Een verhoogde hoeveelheid PSA kán een aanwijzing zijn
voor prostaatkanker. Het kan ook iets zeggen over de uitgebreidheid van een
tumor en de mogelijke
aanwezigheid van uitzaaiingen.
Maar ook bij goedaardige aandoeningen van de prostaat, zoals een infectieuze ontsteking (prostatitis,
zie ook 'Urineweginfecties' in de sectie 'Nieren en Urinewegen') of
prostaatvergroting (BPH, zie ook 'Plasproblemen' in de sectie 'Nieren
& Urinewegen'), kan de PSA-waarde (fors) verhoogd zijn. Daarom is verder onderzoek
noodzakelijk als de PSA-waarde in het bloed hoger is dan 3,0 µg/l (= 3,0 ng/ml). Met de in 2007
op de markt verschenen PCA3-test is men tegenwoordig veel beter in staat
om de aanwezigheid van een agressieve, snel groeiende dan wel een 'slapende'
vorm van prostaatkanker vast te stellen. Met deze nieuwe test kan het aantal
voor de patiënt belastende biopsieën aanzienlijk worden teruggebracht.
Tegenwoordig wordt ook gebruikgemaakt van MRI ('Magnetic Resonance
Imaging') om zowel het stadium als de plaats van de prostaatkanker nauwkeurig in
beeld te brengen, waardoor een effectievere behandeling mogelijk is.

Als is vastgesteld dat de patiënt prostaatkanker heeft, wordt meestal ook nog
een botscan gemaakt om na te gaan of er uitzaaiingen in de botten zijn. Verder
is van
belang om vast te stellen of het om een langzaam groeiende ('slapende')
prostaatkanker gaat dan wel een agressieve, snel groeiende prostaatkanker, die
uitzaaiingen kan geven.
Een slapende prostaatkanker kan doorgaans beter met rust worden gelaten dan dat
er ingrijpend behandeld wordt hetgeen veelal met nare bijwerkingen gepaard gaat.
|
tnm-score
bepaalt tumorstadium
|
|
De
keuze voor een behandeling hangt af van het stadium
waarin de prostaattumor verkeert op het moment van
de diagnose. Dit wordt uitgemaakt met de
tnm-score,
afkomstig van de American Joint Committee on Cancer.
Vijf variabelen wegen daarin mee:
• uitgebreidheid van de primaire tumor (T-categorie);
• uitzaaiing naar de lymfeklieren (N-categorie);
• aanwezigheid van metastasen op afstand (M-categorie);
• psa-concentratie
op het moment van de diagnose;
• de Gleason-score, die is gebaseerd op biopsie of
prostaatweefsel dat is verkregen na chirurgie – deze
score hangt samen met onder meer pathologische
variabelen zoals de tumorgrootte.
Een
laag risico op progressie en dus een betere prognose
hebben patiënten met een lagere
tnm-score
(T1 of T2a), een histologisch goed gedifferentieerde
tumor (Gleasonscore <7) en een
psa
van minder dan 10 μg/l. Van een intermediair risico
is sprake als het carcinoom meer dan de helft van
één prostaatlob of beide lobben beslaat (T2b-c),
matig gedifferentieerd is (Gleason-score 7) en de
psa-concentratie
ligt tussen 10 en 20 μg/l. Een hoog risico is er als
de tumor is uitgebreid buiten de prostaat (T3),
slecht gedifferentieerd is (Gleason-score >7) en de
psa-waarde
> 20 μg/l is. |
Behandeling
Beperkt de ziekte zich tot de prostaat, dan is genezing mogelijk door operatieve
verwijdering van het gezwel of door bestraling (radiotherapie). Dat is het geval
bij ongeveer de helft van de mannen met prostaatkanker. Beide behandelingen
kunnen impotentie en/of incontinentie tot gevolg hebben. Bij de andere helft van
de patiënten heeft de kanker uitzaaiingen veroorzaakt en is de ziekte
ongeneeslijk. Toch kan dan nog veel worden gedaan om de klachten te verminderen
en de groeisnelheid van de kanker af te remmen. Een operatie aan de prostaat kan
de afvoer van urine verbeteren, waardoor de klachten bij het plassen
verminderen. Bestraling kan de botpijn bij uitzaaiingen in botweefsel
verminderen.
Antihormonen
De groeisnelheid kan ook door een hormonale behandeling worden afgeremd. Met de hormonale behandeling
wil men de invloed van het testosteron uitschakelen. Dat gebeurt met de
antihormonen (in dit geval ook wel anti-androgenen
genoemd) abirateron (Zytiga®), bicalutamide (merkloos,
Biluron®, Casodex®), cyproteron (merkloos,
Androcur®),
enzalutamide
(Xtandi®), flutamide (merkloos) of nilutamide (Anandron®),
zie ook antihormonen (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker').
Eenzelfde effect kan worden bereikt met synthetische
hersenhormonen die de secretie van andere hormonen vanuit het
hersenaanhangsel (hypofyse) blokkeren, waardoor de vorming van
testosteron in de teelballen wordt geremd. Voorbeelden van dergelijke stoffen
zijn busereline (Suprefact®), degarelix (Firmagon®),
gosereline (Zoladex®), leuproreline (merkloos,
Eligard®,
Lucrin®) en triptoreline (Decapeptyl®, Pamorelin®,
Salvacyl®,
Triptofem®). Deze aanpak wordt ook
wel chemische castratie genoemd. Een andere mogelijkheid is het operatief
verwijderen van de teelballen (castratie), waardoor de invloed van
testosteron op de kankercellen geheel wegvalt.
Cytostatica
Pas sinds enkele jaren komen sommige patiënten met uitgezaaide prostaatkanker,
bij wie hormoonbehandeling geen effect (meer) heeft, in aanmerking voor een
behandeling met cytostatica, zie voor meer details
cytostatica in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'. Een combinatie van docetaxel (merkloos,
Taxotere®)
en het corticosteroïd prednison (merkloos,
Lodotra®) (zie ook
bijnierschorshormonen
in de sectie 'Hormonen & Stofwisseling') wordt dan meestal gegeven alsmede één van de hierboven
genoemde anti-androgenen om de werking van testosteron geheel te
blokkeren. Als de behandeling aanslaat,
leidt dat tot een iets langere levensduur en een betere kwaliteit van leven.
Indien deze behandeling met docetaxel niet aanslaat, komt het in 2011 op
de markt gebrachte abirateron (Zytiga®) in aanmerking dat de werking van het
testosteron vermindert, zie ook antihormonen in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'). In combinatie met prednison zijn de resultaten
veelbelovend met betrekking tot overlevingswinst, vertraging van de
ziekteprogressie en een milder ziekteverloop.
|
overzicht medicatie
bij prostaatkanker |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Anti-androgenen |
abirateron
bicalutamide
cyproteron
enzalutamide
flutamide
nilutamide |
Zytiga®
merkloos, Biluron®
Casodex®
merkloos, Androcur®
Xtandi®
merkloos
Anandron® |
tablet: 250 mg
tablet: 50 en 150 mg
tablet: 10 en 50 mg
capsule: 40 mg
tablet: 250 mg
tablet: 150 mg |
|
Synthetische hersenhormonen |
busereline
degarelix
gosereline
leuproreline
triptoreline
|
Suprefact®
Firmagon®
Zoladex®
merkloos, Eligard®
Lucrin®
Decapeptyl®, Pamorelin®
Salvacyl®, Triptofem® |
implantatiestift: 9,45 mg
neusspray: 0,1 mg/dosis
injectievloeistof: 80 en 120 mg
implantatiestift: 3,6 en 10,8 mg
implantaat: 3,6 en 5 mg
injectievloeistof: 3,75-45 mg
injectievlst.: 0,5-11,25 mg/ml
|
|
Cytostatica |
|
docetaxel |
merkloos,
Taxotere® |
infusievloeistof: 10-40
mg/ml |
|
Corticosteroïden |
|
prednison |
merkloos,
Lodotra® |
tablet (mga*): 1, 2
en 5 mg |
|
mga* = met gereguleerde afgifte |
De behandeling van prostaatkanker is momenteel volop in ontwikkeling. Zo zijn de
behandeling van prostaatkanker met cryotherapie (het bevriezen van de
tumor, waardoor tumorcellen
afsterven) en met hoogfrequente ultrageluidsgolven (hifu of 'High
Intensity Focused Ultrasound') nieuwe technieken. Onderzocht wordt wat de
waarde is van deze technieken in de curatieve behandeling van
prostaatkanker.
Hoewel bij ongeveer de helft van de patiënten met prostaatkanker genezing
mogelijk is als de ziekte in een vroeg stadium wordt ontdekt, is bij de andere
helft geen genezing meer mogelijk. Door de verschillende
behandelingsmogelijkheden kan de activiteit van de ziekte lange tijd tot staan
worden gebracht. De vijfjaarsoverleving is ongeveer 80 procent. Als er geen
uitzaaiingen
zijn bij het vaststellen van de ziekte, is dit percentage hoger. Als iemand wel
uitzaaiingen heeft, is dit percentage lager.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl (KWF Kankerbestrijding)
http://www.diliguide.nl
(Kwaliteitsinstituut voor de Gezondheidszorg CBO)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Huidkanker
Als alle vormen van huidkanker in de kankerstatistieken zouden worden
meegerekend, zou huidkanker met 36.000 nieuwe gevallen per jaar verreweg de
meest voorkomende vorm van kanker zijn. Ongeveer 80 procent van deze nieuwe
gevallen bestaat gelukkig uit het basaalcelcarcinoom, een vorm van
huidkanker die als minder kwaadaardig wordt beschouwd. Dit carcinoom wordt dan
ook niet meegeteld in de landelijke kankerregistratie. Jaarlijks krijgen
ongeveer 3500 mensen het melanoom, de kwaadaardigste vorm van huidkanker.
In 2007 overleden 661 patiënten aan deze vreselijke ziekte.
Het ontstaan van
huidkanker heeft in veel gevallen te maken met overmatige blootstelling van de
huid aan ultraviolette straling (in zonlicht of van bruiningsapparaten). Mensen
met een van nature lichte huid zijn minder beschermd tegen ultraviolette
straling. Zij hebben de grootste kans om huidkanker te krijgen. Het basaalcelcarcinoom groeit zeer langzaam en zaait vrijwel nooit uit. Het komt
meestal voor in het gezicht. Het plaveiselcelcarcinoom is iets
kwaadaardiger. Ook deze vorm komt nogal eens voor in het gezicht, maar ook op de
rug van de hand.
Melanomen zijn zeer kwaadaardig. Melanoom betekent letterlijk: zwart gezwel. Een
melanoom ontstaat uit de pigmentcellen in de huid: de melanocyten.
Meestal zat er op die plaats al een moedervlek. Soms ontstaat een melanoom uit
pigmentcellen in een volstrekt 'gave' huid. Melanomen ontstaan dus niet alleen
uit moedervlekken. Uitzaaiingen via de lymfe- en bloedvaten komen regelmatig
voor. Het aantal patiënten met een melanoom is de laatste vijftien jaar sterk
toegenomen, mogelijk vanwege een toegenomen blootstelling aan ultraviolette
straling. Meer vrouwen dan mannen krijgen een melanoom. Tegenwoordig wordt bij
de meeste patiënten een melanoom in een relatief vroeg
stadium
vastgesteld.

Bestaat het vermoeden dat het om een melanoom gaat, dan is altijd
weefselonderzoek nodig. De huidtumor moet daarvoor in zijn geheel krap worden
verwijderd. Als er sprake is van een melanoom wordt de dikte van het melanoom
bepaald. Deze zogenoemde Breslow-dikte wordt aangegeven in tienden van
millimeters. Hoe dikker het melanoom, hoe groter het risico op vroege
uitzaaiingen.
Behandeling
Het basaalcelcarcinoom en het plaveiselcelcarcinoom kunnen operatief worden
verwijderd. Tegenwoordig kunnen ze ook worden bestraald, bevroren of weggebrand.
Een andere optie is een lokale behandeling met crème met het cytostaticum
fluorouracil
(Efudix®). Een tweemaaldaagse toediening van de crème gedurende
drie à vier weken geeft vaak een goed resultaat.
De vooruitzichten voor deze vormen van huidkanker zijn heel goed: 95 tot 100 procent van de patiënten geneest
volledig. Een andere optie is een crème met imiquimod (Aldara®,
Zyclara®) - dat ook wordt toegepast bij de behandeling van genitale wratten.
Deze crème dient bij basaalcelcarcinoom 5x per week vóór het slapen gaan te
worden aangebracht op het te behandelen gebied, gedurende 6 weken.
Het melanoom moet vrijwel altijd operatief worden verwijderd. Soms
moeten ook de lymfeklieren in de omgeving van het melanoom worden verwijderd.
Alleen als het melanoom is uitgezaaid, kan worden overwogen chemotherapie toe te
passen, tot voor kort was dat meestal met het cytostaticum dacarbazine (merkloos,
Deticene®). De kans op een
gunstige reactie is echter vrij klein; er is geen duidelijke overlevingswinst. Het immunomodulans interferon-alfa (Intron
A®, Roferan A®) is dan het middel van keuze. De werkzaamheid is echter eveneens niet
erg groot, zie ook
cytostatica en
immunomodulantia (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker').
Sinds 2012 zijn er echter enkele nieuwe middelen geregistreerd die veelbelovend
zijn. Het gaat hier om de zogenaamde proteïnekinaseremmers als dabrafenib (Tafinlar®),
trametinib (Mekinist®) en vemurafenib (Zelboraf®)
en de monoklonale antistoffen als ipilimumab (Yervoy®)
en sinds 2015 nivolumab (Opdivo®) en pembrolizumab (Keytruda®),
zie ook proteïnekinaseremmers
en
monoklonale antistoffen (in het
onderdeel 'Chemotherapie' in deze sectie 'Kanker'). Ze verlengen als eerste geneesmiddelen
de overleving bij het uitgezaaide melanoom met een aantal maanden. De winst is echter nog beperkt.
Bovendien kunnen de bijwerkingen ernstig zijn en zijn de middelen heel erg duur.
Vergelijkbare nieuwe middelen met mogelijk meer effectiviteit en minder
bijwerkingen zijn momenteel in ontwikkeling. De drie hier genoemde
monoklonale antistoffen worden ook wel checkpointremmers
genoemd omdat ze in staat zijn zich te binden aan de afweercelllen (bepaalde
witte bloedcellen) van het immuunsysteem van de patiënt. Vervolgens zorgen ze
ervoor dat de natuurlijke rem van deze cellen wordt 'ontgrendeld' zodat deze de
tumorcellen kunnen opruimen. Kankeronderzoekers en oncologen denken dat
checkpointremmers de kankergeneesmiddelen van de toekomst zullen worden.
|
overzicht medicatie
bij huidkanker |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Cytostatica |
dacarbazine
fluorouracil
imiquimod |
merkloos,
Deticene®
Efudix®
Aldara®, Zyclara® |
injectievloeistof: 200-1000 mg
crème: 50 mg/g
crème: 37,5 en 50 mg/g |
|
Immunomodulantia |
|
interferon-alfa |
Intron
A®,
Roferan A® |
injectievlst.: 6-50 milj. IE/ml |
|
Proteïnekinaseremmers |
dabrafenib
trametinib
vemurafenib |
Tafinlar®
Mekinist®
Zelboraf® |
capsule: 50 en 75 mg
tablet: 0,5 en 2 mg
tablet: 240 mg |
|
Monoklonale antistoffen (checkpointremmers) |
ipilimumab
nivolumab
pembrolizumab |
Yervoy®
Opdivo®
Keytruda® |
infusievloeistof: 5 mg/ml
infusievloeistof: 10 mg/ml
infusievloeistof: 50 mg |
Als het melanoom niet is uitgezaaid, is de kans op genezing bijna 100 procent.
Het gemiddelde overlevingspercentage na vijf jaar is 73 bij mannen en 89 bij
vrouwen. Uitgezaaid melanoom heeft een zeer slechte prognose: een jaar na de
diagnose is de overleving ongeveer 25%.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl (KWF Kankerbestrijding)
http://www.diliguide.nl
(Kwaliteitsinstituut voor de Gezondheidszorg CBO)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Lymfeklierkanker
Lymfeklierkanker (lymfoom of maligne lymfoom) wordt jaarlijks bij ruim 2700 mensen vastgesteld. Er zijn twee
vormen: (de ziekte van) Hodgkin en non-Hodgkin. Het
verschil heeft te maken met welk celtype in de lymfeklieren en lymfevaten gaat
woekeren. Non-Hodgkin komt zesmaal zo vaak voor als Hodgkin.
Een oorzaak voor deze ziekten is nooit gevonden, hoewel men ooit wel eens dacht
aan een virale oorzaak. Voor Hodgkin is een erfelijke component waarschijnlijk.
De klachten beginnen met gezwollen lymfeklieren in hals, oksels of liezen.
Andere klachten bij deze vormen van kanker zijn koorts, moeheid en
gewichtsverlies. Later wordt men ook vatbaarder voor allerlei infecties en
kunnen er bloedingen in de huid, de neus of het tandvlees ontstaan.
Cel- en weefselonderzoek (biopsie) staan centraal bij de diagnose. Op
grond van de resultaten van de hiervoor beschreven onderzoeken kunnen de artsen
vaststellen in welk stadium de ziekte verkeert. Er worden vier stadia
onderscheiden: - stadium I: de ziekte is beperkt tot één lymfekliergebied,
bijvoorbeeld de lymfeklieren in de hals, of tot één orgaan; - stadium II: de
ziekte beperkt zich tot twee of meer kliergebieden boven of onder het middenrif,
of tot één orgaan én een of meer kliergebieden aan dezelfde kant van het
middenrif; - stadium III: de ziekte bevindt zich in kliergebieden boven én onder
het middenrif, en soms ook in de milt en/of een ander orgaan; - stadium IV: de
ziekte heeft zich verspreid naar andere organen die geen lymfeklierweefsel
bevatten, zoals de longen, de lever, het beenmerg of de huid. Bij non-Hodgkin wordt dan ook
nog verschillende typen lymfomen onderscheiden (maar liefst 30-40 verschillende
typen!) en de mate van kwaadaardigheid vastgesteld, hetgeen consequenties heeft
voor de behandeling.
Behandeling
Lymfeklierkanker is doorgaans gevoelig voor zowel bestraling (radiotherapie)
als chemotherapie . Alle Hodgkin-patiënten worden tegenwoordig eerst
met chemotherapie behandeld (in dit geval een combinatie van
cytostatica al dan niet met een
corticosteroïd als prednison (merkloos,
Lodotra®),
zie ook het onderdeel 'Chemotherapie' in deze sectie 'Kanker' en
het onderdeel 'Corticosteroïden'
in de sectie 'Hormonen & Stofwisseling'). Een deel van de patiënten zal daarna ook nog
bestraald worden. Patiënten in de eerste stadia (I en II) hebben meer dan 90
procent kans op genezing. Bij de stadia III en IV varieert dat van 70 tot 80
procent.
Bij de lichtere gevallen van non-Hodgkin (stadium I) heeft lokale bestraling de voorkeur.
Bij de zwaardere gevallen van non-Hodgkin gaat de voorkeur uit naar een combinatie van
bestraling en chemotherapie, meestal een cytostaticum als
chloorambucil (Leukeran®) of een combinatie van cytostatica
met prednison. Tegenwoordig worden ook vaak de monoklonale antistoffen
rituximab (MabThera®) en brentuximab (Adcetris®) toegepast, zie ook
cytostatica en
monoklonale antistoffen (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'). Hoewel peperduur, ontbreken bij
deze middelen de heftige bijwerkingen (met name aantasting van het beenmerg
waardoor een verminderde aanmaak van bloedcellen) van de cytostatica.
Ook de proteïnekinaseremmers als ibrutinib (Imbruvica®)
en idelalisib (Zydelig®) hebben de laatste jaren een belangrijke
plaats ingenomen bij de behandeling van maligne lymfomen.
|
overzicht medicatie
bij lymfeklierkanker |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Cytostatica |
|
chloorambucil |
Leukeran® |
tablet: 2 mg |
|
Corticosteroïden |
|
prednison |
merkloos,
Lodotra® |
tablet (mga*): 1, 2
en 5 mg |
|
Monoklonale antistoffen |
rituximab
brentuximab |
MabThera®
Adcetris® |
infusievloeistof: 10 mg/ml
injectievloeistof: 120 mg/ml
infusievloeistof: 50 mg |
|
Proteïnekinaseremmers |
ibrutinib
idelalisib |
Imbruvica®
Zydelig® |
capsule:
140 mg
tablet: 100 en 150 mg |
|
mga* = met gereguleerde afgifte |
Overigens wordt na intensieve chemotherapie, al dan niet in combinatie met
bestraling, stamceltransplantatie toegepast. Dit om het herstel te
versnellen van de beschadigde beenmergcellen (zie ook
stamceltransplantatie
in de 'Inleiding' van de sectie 'Kanker'). De vijfjaarsoverleving
van patiënten met non-Hodgkin-patiënten is ongeveer 50 procent.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl/non-Hodgkin (KWF Kankerbestrijding)
https://www.kanker.nl/Hodgkin (KWF Kankerbestrijding)
http://www.diliguide.nl
(Kwaliteitsinstituut voor de Gezondheidszorg CBO)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Blaaskanker
Elk jaar worden in Nederland bijna 7000 nieuwe gevallen van blaaskanker ontdekt.
Daarbij zijn zowel de oppervlakkige als de diepere (invasieve) vormen meegeteld.
Blaaskanker ontstaat bij mannen driemaal zo vaak als bij vrouwen. Roken is een
belangrijke risicofactor bij minstens de helft van de patiënten. Chronische
irritatie, bijvoorbeeld door bepaalde worminfecties of blaasstenen, vergroot de
kans op het ontstaan van blaaskanker.
Soms wordt blaaskanker bij toeval ontdekt doordat er rode bloedcellen in de
urine aanwezig zijn. Meestal ontstaan de typische verschijnselen van een
blaasontsteking (in
het onderdeel 'Urineweginfecties' in de sectie 'Nieren &
Urinewegen'): brandende pijn bij het plassen en een frequente, sterke
aandrang om te plassen. Via een cystoscoop (blaasspiegel die via de
plasbuis in de blaas wordt geschoven ter inspectie en om monsters van verdacht
weefsel te nemen) kan een beeld worden verkregen van de afwijkingen.
Er zijn verschillende stadia van blaaskanker te onderscheiden. Als de tumor zich
alleen in het slijmvliesweefsel van de blaas bevindt, wordt gesproken van een
niet-spierinvasief groeiende tumor. Bij ongeveer driekwart van de patiënten gaat het
om een dergelijk oppervlakkig groeiende vorm. Wanneer een niet-spierinvasief
groeiende tumor niet tijdig wordt behandeld en agressief van aard is, zal deze
op den duur doorgroeien in de blaasspier. Dan ontstaat een spierinvasief
groeiende tumor. Wanneer de tumor is ingegroeid in de diepere lagen van de
blaaswand, wordt het risico groter dat er kankercellen losraken die vervolgens
in het lichaam worden verspreid. Via de lymfevaten kunnen losgeraakte
kankercellen terechtkomen in de lymfeklieren rond de blaas en ergens anders in
het lichaam. Op deze wijze kunnen uitzaaiingen in de lymfeklieren ontstaan. Bij
verspreiding via het bloed kunnen uitzaaiingen ontstaan in organen als de lever,
longen en de botten.

Behandeling
Bij de niet-spierinvasieve vorm van blaaskanker kan met behulp
van de cystoscoop oppervlakkige tumoren aan de binnenkant van
de blaas worden weggenomen. Deze methode wordt ook wel een transurethrale
resectie (TUR) genoemd. Na een TUR is er een aanzienlijk risico (60 tot 70%)
dat de tumor binnen een jaar terugkeert. Om het risico op een terugkeer (recidief)
te verminderen, is soms een aanvullende (adjuvante) behandeling
nodig. Meestal bestaat zo'n behandeling uit een of meer blaasspoelingen.
Daarna duurt het langer voordat de tumor terugkeert. Voor een blaasspoeling
wordt eerst een blaaskatheter ingebracht. Via de katheter loopt alle urine uit
de blaas. Daarna worden medicijnen, die opgelost zijn in een vloeistof, in de
blaas gebracht. Na het inbrengen van de medicijnen wordt de katheter meteen weer
verwijderd en kan de vloeistof met de medicijnen na verloop van tijd gewoon
uitgeplast worden. Het cytostaticum mitomycine (merkloos,
Mitomycin-C®) of de immunomodulantia BCG-vaccin (Oncotice®)
en immunocyanine (Immucothel®) zijn werkzaam bij deze oppervlakkige
tumoren van de blaas, zie ook
cytostatica en
immunomodulantia (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'). Wanneer er telkens kleine, nieuwe tumoren gevonden worden
kan een laserbehandeling worden gegeven. De gerichte laserstralen zorgen ervoor
dat de tumorcellen als het ware verdampen. Net als bij een TUR vindt een
laserbehandeling plaats met een cystoscoop via de plasbuis.
Kankergezwellen die diep in of door de blaaswand zijn gegroeid - de
spierinvasieve vormen dus -
worden behandeld door de blaas geheel of gedeeltelijk weg te nemen. Soms wordt
het gezwel intensief bestraald voordat de operatie wordt uitgevoerd. Als de
blaas volledig wordt verwijderd, moet in de buikwand een andere uitgang (stoma)
voor de urine worden gemaakt. Soms wordt een intensieve bestraling gecombineerd
met een kuur van een cytostaticum meestal cisplatine (merkloos).
Maar vaak zijn cytostatica niet erg effectief
bij deze vormen van blaaskanker. Alleen als de kanker is uitgezaaid wordt intensieve
chemotherapie overwogen: ook hier cisplatine maar nu in combinatie met
gemcitabine (merkloos).
|
overzicht medicatie
bij blaaskanker |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Cytostatica |
cisplatine
gemcitabine
mitomycine |
merkloos
merkloos
merkloos, Mitomycin-C® |
infusievloeistof:
1 mg/ml
infusievloeistof: 200-2000
mg
injectievloeistof: 2 en 40 mg |
|
Immunomodulantia |
BCG-vaccin
immunocyanine
|
merkloos,
Oncotice®
Immucothel®
|
instillatievloeistof
injectievloeistof: 1 mg
instillatievloeistof: 10 mg |
De vijfjaarsoverleving van patiënten met de niet-spierinvasieve vorm van
blaaskanker is ongeveer 70 tot 90%, terwijl die van patiënten met de spierinvasieve
vormen aanzienlijk lager is: 30 tot 60%. Indien er sprake is van uitzaaiingen
elders in het lichaam is de vijfjaarsoverleving ongeveer 10%.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl (KWF Kankerbestrijding)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Maagkanker
Hoewel maagkanker in Nederland steeds minder voorkomt, wordt deze diagnose
jaarlijks bij ruim 2000 mensen gesteld. Mannen krijgen bijna tweemaal zo vaak
maagkanker
als vrouwen.
Bepaalde voedingsmiddelen hebben invloed op het ontstaan van maagkanker. In
landen waar veel wordt gerookt en gezouten vlees en vis worden gegeten in combinatie
met
weinig verse groenten en fruit, komt maagkanker veel vaker voor. Maagpoliepen of
een chronische ontsteking van de maag zijn eveneens factoren die het risico op
het
ontstaan van maagkanker verhogen.
De klachten kunnen bestaan uit moeheid, lusteloosheid en duizeligheid door
bloedarmoede
(als gevolg van bloedverlies uit het kankergezwel in de maag), gewichtsverlies,
weinig eetlust, pijn in de maagstreek en misselijkheid. Deze klachten komen vaak
pas
in een relatief laat stadium van maagkanker voor. Onderzoek van bloed en
ontlasting,
röntgenfoto’s van de maag, inwendig kijkonderzoek (gastroscopie) en
weefselonderzoek
zijn technieken om de diagnose te kunnen stellen.
Behandeling
Volledige genezing is alleen mogelijk als het kankergezwel volledig wordt
verwijderd.
Dat is alleen mogelijk als het gezwel nog niet al te ver is doorgegroeid. De
operatie is
altijd zwaar en erg belastend. Als het gezwel tot buiten de maag is doorgegroeid,
zal de
patiënt behandeld moeten worden met bestraling of chemotherapie, of met een
combinatie van beide. Bij de aanwezigheid van uitzaaiingen op afstand is alleen
palliatieve chemotherapie nog een mogelijkheid. Cytostatica zijn overigens niet erg effectief bij
maagkanker. Desondanks worden combinaties van cisplatine
(merkloos)
met fluorouracil (merkloos), carboplatine (merkloos,
Carbosin®)
met paclitaxel (merkloos,
Abraxane®, Paclitaxin®) of oxaliplatine (merkloos,
Oxalisin®) met capecitabine (merkloos,
Xeloda®) gebruikt,
zie ook
cytostatica (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker').
|
overzicht medicatie
bij maagkanker |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Cytostatica |
capecitabine
carboplatine
cisplatine
fluorouracil
oxaliplatine
paclitaxel
|
merkloos,
Xeloda®
merkloos, Carbosin®
merkloos
merkloos
merkloos,
Oxalisin®
merkloos, Abraxane®
Paclitaxin® |
tablet: 150,
300 en 500 mg
infusievloeistof: 10 mg/ml
infusievloeistof:
1 mg/ml
injectievloeistof: 50 mg/ml
infusievloeistof: 5 mg/ml
infusievloeistof: 6 mg/ml,
100 mg
|
De vijfjaarsoverleving van patiënten met maagkanker is slechts 20 procent.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl (KWF Kankerbestrijding)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Nierkanker
Nierkanker wordt jaarlijks bij ongeveer 1700
mensen
vastgesteld; bij mannen anderhalf keer vaker dan bij vrouwen. In 90-95% gaat het
om het niercelcarcinoom (vroeger Grawitz-tumor genoemd). Over de oorzaak is
niets
bekend. Bij slechts 1 procent van de patiënten ontstaat de ziekte door erfelijke
aanleg.
Bloed in de urine is de meest voorkomende eerste klacht, met daarnaast pijn in
de zij
en koorts. Nierkanker kan ook bij toeval worden ontdekt als een arts bij
routineonderzoek een zwelling of knobbeltje in de buik voelt. Voor het stellen van de
definitieve
diagnose kan de arts beschikken over technieken als urografie (röntgenonderzoek
van de
nieren en urinewegen na inspuiting van een contrastmiddel), echografie en
computertomografie
(CT-scan: computergestuurd röntgenonderzoek naar structurele afwijkingen).
Behandeling
Als er geen uitzaaiingen buiten de nier zijn, is de kans op genezing redelijk
groot na
operatieve verwijdering van de aangetaste nier en de lymfeklieren. Een groot
probleem
is dat nierkanker zich in een vroeg stadium uitzaait, vooral naar de longen. In
dat geval is
het vooruitzicht slecht, omdat bestraling en chemotherapie weinig effect hebben
in dit
stadium van de ziekte. Sinds kort worden echter bescheiden resultaten geboekt
met de immunomodulantia aldesleukin (Proleukin®) of
interferon-alfa (Intron A®,
Roferon A®) in combinatie met het cytostaticum vinblastine (merkloos,
Blastivin®). Ook de monoklonale antistoffen
bevacizumab (Avastin®) en nivolumab (Opdivo®) komen in aanmerking, met name als er sprake
is van uitzaaiingen, zie ook
cytostatica,
immunomodulantia en
monoklonale antistoffen (in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'). Als deze middelen onvoldoende resultaat boeken, kunnen nog de
proteïnekinaseremmers axitinib (Inlyta®), everolimus (Afinitor®,
Votubia®), pazopanib (Votrient®), sorafenib (Nexavar®),
sunitinib (Sutent®) of temsirolimus (Torisel®) worden ingezet,
zie ook proteïnekinaseremmers
(in het onderdeel 'Chemotherapie' in deze sectie 'Kanker').
|
overzicht medicatie
bij nierkanker |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Cytostatica |
|
vinblastine |
merkloos,
Blastivin® |
injectievloeistof: 1 mg/ml |
|
Immunomodulantia |
aldesleukin
interferon-alfa |
Proleukin®
Intron A®, Roferon A® |
injectievloeistof: 22.106
IE
injectievlst.: 6-50 milj. IE/ml |
|
Monoklonale antistoffen |
bevacizumab
nivolumab |
Avastin®
Opdivo® |
infusievloeistof: 25 mg/ml
infusievloeistof: 10 mg/ml |
|
Proteïnekinaseremmers |
axitinib
everolimus
pazopanib
sorafenib
sunitinib
temsirolimus |
Inlyta®
Afinitor®, Votubia®
Votrient®
Nexavar®
Sutent®
Torisel® |
tablet:
1, 3, 5 en 7 mg
tablet:
2½, 5 en 10 mg
suspensie (als tablet): 5 mg
tablet: 200 en 400 mg
tablet: 200 mg
capsule: 12½, 25 en 50 mg
infusievloeistof: 25 mg/ml |
De vijfjaarsoverleving van patiënten met nierkanker zonder uitzaaiingen is 40
tot 60 procent; mét uitzaaiingen is die 10 tot 15 procent.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl (KWF Kankerbestrijding)
http://www.diliguide.nl
(Kwaliteitsinstituut voor de Gezondheidszorg CBO)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Leukemie
Leukemie is een verzamelnaam van in principe vier vormen van kanker van witte
bloedcellen (leukocyten en lymfocyten). Er wordt onderscheid gemaakt tussen
acute
(snel verlopende) en chronische (langzaam verlopende) leukemie. Daarnaast is het
onderscheid
tussen lymfatische en myeloïde leukemie van belang. Dit onderscheid heeft
te maken met het type witte bloedcellen dat is gaan woekeren.
Het aantal nieuwe gevallen van leukemie is ongeveer 1600 per jaar. Acute
lymfatische
leukemie treft vooral kinderen, terwijl acute myeloïde leukemie en de chronische
vormen
van leukemie vooral bij volwassenen en ouderen voorkomen. In 25 procent van alle
gevallen van kanker bij kinderen gaat het om acute lymfatische leukemie. De
ziekte komt
het meest voor bij kinderen tussen 3 en 5 jaar.
Meestal is de oorzaak van leukemie niet bekend. Toch zijn er enkele factoren
waarvan
vaststaat dat ze een rol spelen bij het ontstaan van leukemie, namelijk
radioactieve
straling en sommige chemische stoffen (benzeen, pesticiden, insecticiden).
Mogelijk
zijn ook erfelijke factoren van belang. Vroegere behandelingen met cytostatica
kunnen
vele (tientallen) jaren later leukemie veroorzaken.
Moeheid, infecties, koorts en spontane bloedingen zijn de eerste klachten bij
acute
leukemie. Ze hebben alle te maken met een gestoorde aanmaak van witte en rode
bloedcellen.
Het ziektebeeld bij chronische leukemie is veel sluipender. Bij deze klachten
staan
het lichamelijk onderzoek en bloedonderzoek centraal, aangevuld met
beenmergonderzoek
om afwijkende cellen aan te tonen.
Behandeling
Zowel het onderscheid tussen acute en chronische leukemie als het verschil
tussen
lymfatische en myeloïde leukemie zijn van belang voor de keuze van de
behandeling.
Acute lymfatische leukemie bij kinderen kan in veel gevallen volledig worden
genezen.
Chemotherapie
Het effectiefst bij de behandeling van acute lymfatische leukemie (ALL) is chemotherapie in de vorm van combinaties van cytostatica en
corticosteroïden (zie ook
cytostatica in het onderdeel 'Chemotherapie' in deze sectie 'Kanker'
en bijnierschorshormonen
in de sectie 'Hormonen & Stofwisseling').
Meestal geeft men de cytostatica vincristine (merkloos), daunorubicine (Cerubidine®),
cyclofosfamide
(Endoxan®), asparaginase (Erwinase®, Paronal®) en cytarabine (merkloos,
DepoCyte®) in combinatie met het corticosteroïd
prednison (merkloos,
Lodotra®),
maar
ook andere combinaties zijn effectief. Bij meer dan 80 procent van de kinderen
wordt
de ziekte met zo’n eerste chemokuur onder controle gebracht. Toch kan de ziekte
dan
wel terugkomen. Daarom volgt meestal een onderhoudsbehandeling die hooguit twee
jaar duurt. Tegenwoordig wordt in plaats daarvan ook wel een beencel- of
stamceltransplantatie
(zie ook stamceltransplantatie
in de 'Inleiding' van de sectie 'Kanker')
uitgevoerd. Bij oudere kinderen en jonge volwassenen is de behandeling
meestal wat minder succesvol. Acute myeloïde leukemie (AML), meestal bij volwassenen
optredend,
is
veel moeilijker te behandelen. Ook dan is chemotherapie de behandeling van
keuze,
vaak gevolgd door een beenmerg- en stamceltransplantatie.
Monoklonale antistoffen
Chronische vormen van leukemie
zijn
meestal nog moeilijker te behandelen, maar soms is geen behandeling nodig door
het trage verloop van de ziekte. Sinds een aantal jaren kan chronische lymfatische leukemie
(CLL)
worden behandeld met bepaalde monoklonale antistoffen zoals rituximab (MabThera®),
zie ook monoklonale antistoffen
in het onderdeel 'Chemotherapie' van deze sectie 'Kanker'). Maar alleen als gebleken is dat de
behandeling met alkylerende cytostatica onvoldoende werkzaam is.
Proteïnekinaseremmers
Deze stoffen inactiveren het enzym
proteïnekinase, dat aan de basis ligt van de abnormale toename van de
bloedcellen. Met die behandeling kan het kenmerkende mechanisme van
chronische myeloïde leukemie (CML) worden geblokkeerd.
De proteïnekinaseremmers vormen tegenwoordig de belangrijkste
behandeling van deze vorm van bloedkanker. De introductie van imatinib (Glivec®)
in 2001 heeft de prognose van patiënten met CML enorm verbeterd. Zo was meer dan
negentig procent van de patiënten die werd behandeld met imatinib in de
grote klinische studie na acht jaar nog in leven. Sinds enkele jaren vormen de
nieuwe potentere tweedegeneratie proteïnekinaseremmers als nilotinib (Tasigna®) en dasatinib (Sprycel®)
een therapeutisch alternatief. In 2014 werden bosutinib (Bosulif®)
en ponatinib (Iclusig®) aan het therapeutisch arsenaal
toegevoegd. Ibrutinib
(Imbruvica®)
en idelalisib
(Zydelig®) worden voorlopig nog als enige protïnekinaseremmers bij de behandeling van chronische
lymfatische leukemie toegepast. Imatinib wordt tegenwoordig ook bij
acute lymfatische leukemie ingezet.
De belangrijkste bijwerkingen van deze proteïnekinaseremmers zijn
misselijkheid, spierkrampen, oedeem, hoofdpijn, vermoeidheid,
gewrichtsklachten, huiduitslag,
leverfunctiestoornissen, zie ook
proteïnekinaseremmers in
het onderdeel 'Chemotherapie' in deze sectie 'Kanker'.
VENETOCLAX
In 2017 werd een erg interessant, nieuw medicijn tegen chronische
lymfatische leukemie (CLL) geïntroduceerd met de naam venetoclax (Venclyxto®).
Hoewel CLL de minst agressieve vorm van leukemie is (het doet er jaren over om
levensbedreigend te worden), is het in Nederland de leukemie met de meeste
nieuwe patiënten: jaarlijks ongeveer 600. Venetoclax, hecht zich aan een
eiwit, BCL-2. Dit eiwit is bij CLL in grote hoeveelheden aanwezig in
kankercellen, waar het de cellen helpt om langer in het lichaam te overleven en
ze resistent maakt voor medicijnen tegen kanker. Door zich aan BCL-2 te hechten
en de effecten hiervan te blokkeren, zorgt venetoclax ervoor dat
kankercellen afsterven en vertraagt het de progressie van de ziekte. Uit diverse
studies is gebleken dat bij een hoog percentage (67-85%) patiënten de
kankercellen gedeeltelijk of volledig zijn verdwenen na behandeling met
venetoclax terwijl twee jaar lang de ziekte niet erger werd.
Het middel wordt oraal (dus via de mond) dagelijks via tabletten
toegediend. De startdosis is laag en wordt gedurende vijf weken geleidelijk
verhoogd. De patiënt dient met de behandeling door te gaan zolang hij of zij een
verbetering vertoont of stabiel blijft en de bijwerkingen te verdragen zijn. Als
de patiënt bepaalde bijwerkingen ondervindt, kan de behandeling tijdelijk worden
stopgezet of kan de dosis worden verlaagd. De meest voorkomende bijwerkingen
zijn een verminderd aantal neutrofielen (een type witte bloedcel),
diarree, misselijkheid, bloedarmoede, neus- en keelinfectie, vermoeidheid, hoge
concentratie fosfaat in het bloed, braken en verstopping. Ernstiger bijwerkingen
zijn longinfecties, koorts in verband met een verminderd aantal neutrofielen en
tumorlysissyndroom (een complicatie veroorzaakt door afbraak van
kankercellen).
Kankerspecialisten zijn van oordeel dat met dit middel een enorme
stap voorwaarts is gemaakt bij de behandeling van CLL. De keerzijde is dat er
net als bij zo vele andere nieuwe kankermiddelen een fors prijskaartje aanhangt:
ruim € 6000 per maand, d.w.z. zo'n € 70.000,- per patiënt per jaar. Voorlopig
mag venetoclax dan ook alleen voorgeschreven worden bij CLL-patiënten
wanneer andere behandelingen hebben gefaald of ongeschikt zijn.
|
overzicht medicatie
bij leukemie |
|
stofnaam |
merknaam® |
toedieningsvorm:
sterkte |
|
Cytostatica |
asparaginase
cyclofosfamide
cytarabine
daunorubicine
vincristine |
Erwinase®, Paronal®
Endoxan®
merkloos, DepoCyte®
Cerubidine®
merkloos |
injectievloeistof: 10.000 IE
injectievloeistof:
750 en 2000 mg
tablet: 50 mg
injectievloeistof: 10-100
mg/ml
injectievloeistof: 20 mg
injectievloeistof:
1 mg/ml |
|
Corticosteroïden |
|
prednison |
Lodotra® |
tablet (mga*): 1, 2
en 5 mg |
|
Monoklonale antistoffen |
|
rituximab |
Mabthera® |
infusievloeistof: 10 mg/ml
injectievloeistof: 120 mg/ml |
|
proteïnekinaseremmers |
bosutinib
dasatinib
ibrutinib
idelalisib
imatinib
nilotinib
ponatinib |
Bosulif®
Sprycel®
Imbruvica®
Zydelig®
Glivec®
Tasigna®
Iclusig® |
tablet:
100 en 500 mg
tablet: 20, 50, 70 en 100 mg
capsule: 140 mg
tablet: 100 en 150 mg
capsule/tablet: 100 en 400 mg
capsule: 150 en 200 mg
tablet: 15 en 45 mg |
|
VENETOCLAX |
|
venetoclax |
Venclyxto® |
tablet: 10, 50
en 100 mg |
|
mga* = met gereguleerde afgifte |
Voor de totale groep mensen met acute lymfatische
leukemie
is een vijfjaarsoverleving te verwachten van ongeveer 30%. De meeste kinderen
(meer dan 80%) met acute lymfatische leukemie genezen volledig. Voor de
totale groep mensen met acute myeloïde leukemie is de vijfjaarsoverleving circa
20%.

Externe links:
https://www.apotheek.nl
(Apotheek.nl; KNMP)
https://www.kanker.nl (KWF Kankerbestrijding)
http://www.farmacotherapeutischkompas.nl
(Farmacotherapeutisch Kompas)
Terug |
 In 90 procent van de gevallen beginnen de kankercellen te groeien in het
melkklierweefsel van de borst. Na verloop van tijd kunnen de kwaadaardige cellen
doorgroeien in het weefsel dat de melkkliertjes omringt. Als ze losraken, kunnen
uitzaaiingen ontstaan in de lymfeklieren van de oksel. In een latere fase kunnen
ook in andere weefsels en organen uitzaaiingen voorkomen, zoals longen, botten,
hersenen, lever en huid.
In 90 procent van de gevallen beginnen de kankercellen te groeien in het
melkklierweefsel van de borst. Na verloop van tijd kunnen de kwaadaardige cellen
doorgroeien in het weefsel dat de melkkliertjes omringt. Als ze losraken, kunnen
uitzaaiingen ontstaan in de lymfeklieren van de oksel. In een latere fase kunnen
ook in andere weefsels en organen uitzaaiingen voorkomen, zoals longen, botten,
hersenen, lever en huid.





